Page 162 - 883351_podrecznik chemia_kl7_nowaPP
P. 162
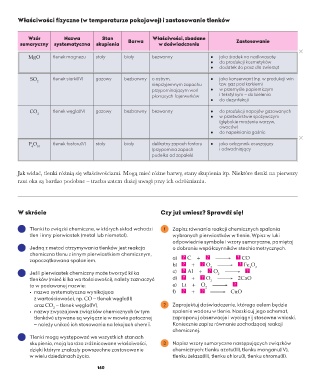
Właściwości fizyczne (w temperaturze pokojowej) i zastosowanie tlenków
Wzór Nazwa Stan Właściwości, zbadane
Barwa Zastosowanie
sumaryczny systematyczna skupienia w doświadczeniu
MgO tlenek magnezu stały biały bezwonny • jako środek na nadkwasotę
• do produkcji kosmetyków
• dodatek do pasz dla zwierząt
SO tlenek siarki(IV) gazowy bezbarwny o ostrym, • jako konserwant (np. w produkcji win
2
nieprzyjemnym zapachu tzw. gaz pod korkiem)
przypominającym woń • w przemyśle papierniczym
płonących fajerwerków • i tekstylnym − do bielenia
do dezynfekcji
CO 2 tlenek węgla(IV) gazowy bezbarwny bezwonny • do produkcji napojów gazowanych
•
w przetwórstwie spożywczym
(głębokie mrożenie warzyw,
• owoców)
do napełniania gaśnic
P O 10 tlenek fosforu(V) stały biały delikatny zapach fosforu • jako odczynnik osuszający
4
(przypomina zapach i odwadniający
pudełka od zapałek)
Jak widać, tlenki różnią się właściwościami. Mogą mieć różne barwy, stany skupienia itp. Niektóre tlenki na pierwszy
rzut oka są bardzo podobne – trzeba zatem dużej uwagi przy ich odróżnianiu.
W skrócie Czy już umiesz? Sprawdź się!
Tlenki to związki chemiczne, w których skład wchodzi 1 Zapisz równania reakcji chemicznych spalania
tlen i inny pierwiastek (metal lub niemetal). wybranych pierwiastków w tlenie. Wpisz w luki
odpowiednie symbole i wzory sumaryczne, pamiętaj
Jedną z metod otrzymywania tlenków jest reakcja o dobraniu współczynników stechiometrycznych.
chemiczna tlenu z innym pierwiastkiem chemicznym, ? C + ? ? CO
zapoczątkowana spalaniem. a)
b) ? + ? O ? Fe O 3
2
2
Jeśli pierwiastek chemiczny może tworzyć kilka c) ? Al + ? O ?
2
tlenków (mieć kilka wartościowości), należy zaznaczyć d) ? + ? O 2CaO
2
to w podawanej nazwie: e) Li + O ?
2
• nazwa systematyczna wynikająca f) ? + ? CuO
z wartościowości, np. CO – tlenek węgla(II)
oraz CO – tlenek węgla(IV), 2 Zaprojektuj doświadczenie, którego celem będzie
2
• nazwy zwyczajowe związków chemicznych (w tym spalenie wodoru w tlenie. Naszkicuj jego schemat,
tlenków) używane są wyłącznie w mowie potocznej zaproponuj obserwacje i wyciągnij stosowne wnioski.
– należy unikać ich stosowania na lekcjach chemii. Koniecznie zapisz równanie zachodzącej reakcji
chemicznej.
Tlenki mogą występować we wszystkich stanach
skupienia, mają bardzo zróżnicowane właściwości, 3 Napisz wzory sumaryczne następujących związków
dzięki którym znalazły powszechne zastosowanie chemicznych: tlenku azotu(III), tlenku manganu(IV),
w wielu dziedzinach życia. tlenku żelaza(III), tlenku chloru(I), tlenku chromu(II).
160