Page 83 - chemia_k8
P. 83
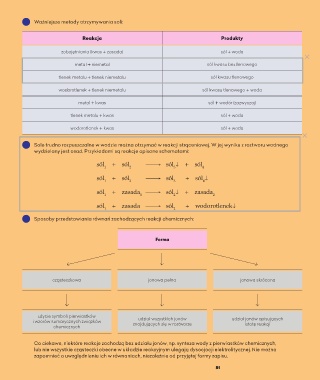
Ważniejsze metody otrzymywania soli:
Reakcja Produkty
zobojętniania (kwas + zasada) sól + woda
metal + niemetal sól kwasu beztlenowego
tlenek metalu + tlenek niemetalu sól kwasu tlenowego
wodorotlenek + tlenek niemetalu sól kwasu tlenowego + woda
metal + kwas sól + wodór (zazwyczaj)
tlenek metalu + kwas sól + woda
wodorotlenek + kwas sól + woda
Sole trudno rozpuszczalne w wodzie można otrzymać w reakcji strąceniowej. W jej wyniku z roztworu wodnego
wydzielany jest osad. Przykładami są reakcje opisane schematami:
sól + sól sól ↓ + sól
1 2 3 4
sól + sól sól + sól ↓
1 2 3 4
sól + zasada 1 sól ↓ + zasada 2
1
2
sól + zasada sól + wodorotlenek ↓
1 2
Sposoby przedstawiania równań zachodzących reakcji chemicznych:
Forma
cząsteczkowa jonowa pełna jonowa skrócona
użycie symboli pierwiastków
udział wszystkich jonów
i wzorów sumarycznych związków znajdujących się w roztworze udział jonów opisujących
istotę reakcji
chemicznych
Co ciekawe, niektóre reakcje zachodzą bez udziału jonów, np. synteza wody z pierwiastków chemicznych,
lub nie wszystkie cząsteczki obecne w układzie reakcyjnym ulegają dysocjacji elektrolitycznej. Nie można
zapomnieć o uwzględnieniu ich w równaniach, niezależnie od przyjętej formy zapisu.
81
10.06.2021 11:48:52
0610_881399_chemia_kl8_podrecznik_DRUK.indd 81
0610_881399_chemia_kl8_podrecznik_DRUK.indd 81 10.06.2021 11:48:52