Page 156 - chemia_k8
P. 156
Jak otrzymać etanian etylu?
Doświadczenie 31.
Ogrzewanie mieszaniny kwasu octowego, etanolu i kwasu siarkowego(VI)
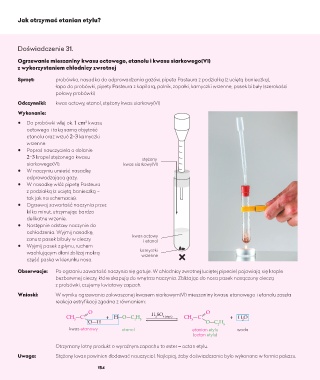
z wykorzystaniem chłodnicy zwrotnej
Sprzęt: probówka, nasadka do odprowadzania gazów, pipeta Pasteura z podziałką (z uciętą banieczką),
łapa do probówki, pipety Pasteura z kapilarą, palnik, zapałki, kamyczki wrzenne, pasek bibuły (szerokości
połowy probówki)
Odczynniki: kwas octowy, etanol, stężony kwas siarkowy(VI)
Wykonanie:
• Do probówki wlej ok. 1 cm kwasu
3
octowego i taką samą objętość
etanolu oraz wrzuć 2−3 kamyczki
wrzenne.
• Poproś nauczyciela o dolanie
2−3 kropel stężonego kwasu stężony
siarkowego(VI). kwas siarkowy(VI)
• W naczyniu umieść nasadkę
odprowadzającą gazy.
• W nasadkę włóż pipetę Pasteura
z podziałką (z uciętą banieczką –
tak jak na schemacie).
• Ogrzewaj zawartość naczynia przez
kilka minut, utrzymując bardzo
delikatne wrzenie.
• Następnie odstaw naczynie do
ochłodzenia. Wyjmij nasadkę,
zanurz pasek bibuły w cieczy. kwas octowy
i etanol
• Wyjmij pasek z płynu, ruchem
wachlującym dłoni zbliżaj mokrą kamyczki
wrzenne
część paska w kierunku nosa.
Obserwacje: Po ogrzaniu zawartość naczynia się gotuje. W chłodnicy zwrotnej (uciętej pipecie) pojawiają się krople
bezbarwnej cieczy, które skapują do wnętrza naczynia. Zbliżając do nosa pasek nasączony cieczą
z probówki, czujemy kwiatowy zapach.
Wnioski: W wyniku ogrzewania zakwaszonej kwasem siarkowym(VI) mieszaniny kwasu etanowego i etanolu zaszła
reakcja estryfi kacji zgodna z równaniem:
O H SO O
CH C + H O C H 2 4 (stęż.) CH C + H O
3
O H 2 5 3 O C H 2
2 5
kwas etanowy etanol etanian etylu woda
(octan etylu)
Otrzymany lotny produkt o wyraźnym zapachu to ester – octan etylu.
Uwaga: Stężony kwas powinien dodawać nauczyciel. Najlepiej, żeby doświadczenie było wykonane w formie pokazu.
154
10.06.2021 11:50:39
0610_881399_chemia_kl8_podrecznik_DRUK.indd 154
0610_881399_chemia_kl8_podrecznik_DRUK.indd 154 10.06.2021 11:50:39